在制药行业里,呼吸器滤芯是保障无菌工艺与环境安全的第一道防线,在生物技术行业中亦是如此,在食品饮料等行业内同样是这样。完整性测试并非单纯的“过一遍水”那般,而是一项必须严谨执行的关键质控环节。它直接关联到生产过程的合规性,它直接关系到产品的无菌保障,它还直接影响终能否通过GMP检查。很多现场人员在实际操作期间会碰到测试方法选择的具体问题,很多现场人员在实际操作之中会遇到结果判断的具体问题,很多现场人员在实际操作过程中会遭遇故障排查的具体问题,下面我们就从几个核心维度展开。
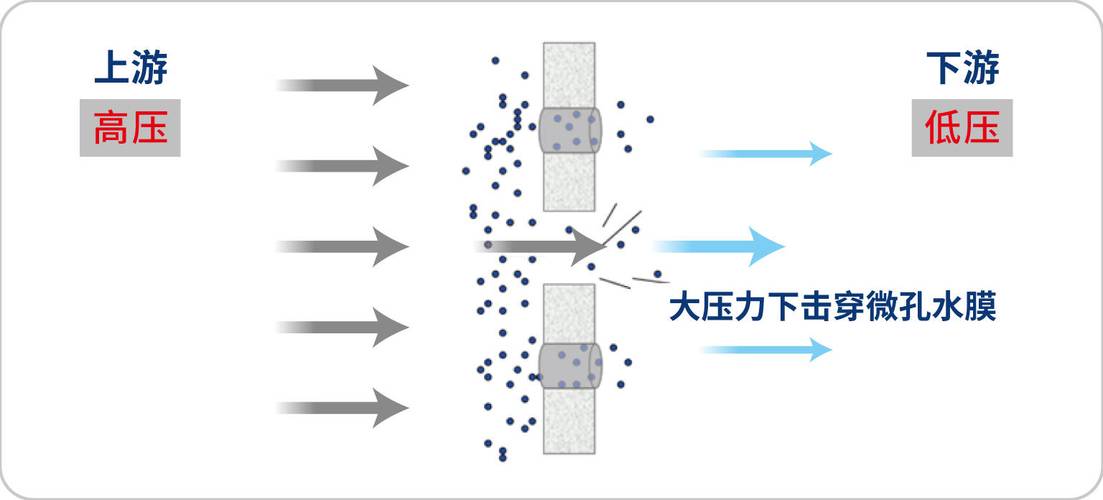
当代主流的完整性测试办法涵盖起泡点测试、扩散流测试以及水侵入法,起泡点测试适用利于水之类而亲近的滤芯,凭借监测气体突破膜孔之际的压力数值来判定结构完备性,对于疏水性滤芯,像呼吸器常常运用的聚四氟乙烯材质,提议优先选用水侵入法,其能够直观展现滤芯在被湿润状况下的完整情形,扩散流测试则更着重于定量评估气体透过湿润膜孔的扩散流量,适宜对精度拥有较高要求的场景,挑选方法之时要结合滤芯材质、孔径以及实际工艺需求。
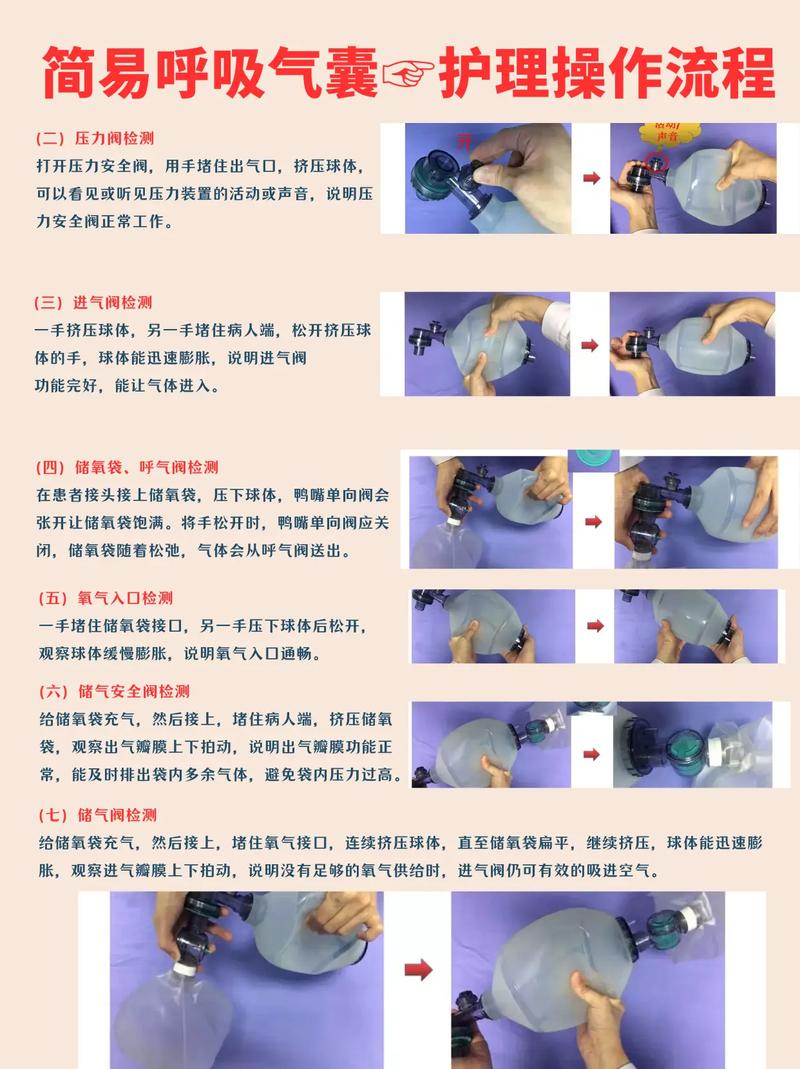
测试之前的准备工作会对结果可靠性造成直接影响,首先得去确认滤芯安装方向是正确的,密封圈不存在老化破损情况,同时要确保滤壳是拥有测试接口的,那润湿液的选择这件事是非常关键重要的,一般而言会去使用纯化水或者注用水,必须要保证水质的电导率能够达到标准,并且温度稳定处在20至25℃这个范围,操作人员应该提前对测试仪器的压力传感器以及流量计进行校准,并且要依据滤芯生产商所提供的技术参数来设定测试限值,现场环境也是需要加以留意的,要防止振动以及气流扰动对高精度测量造成干扰。
进行测试时,一旦失败,常常会致使相关人员感到极为头疼,不过,在大多数情形下,是能够找寻到清晰明确的原因的。经常出现的状况,就是滤芯并未完全被润湿好,进而使得气体提前就穿透过去了,终形成了假阳性的结果,针对这种情况,可以再次去执行润湿这一步骤,并且延长浸泡所需要的时间。另外,要是密封圈安装得不合适,或者滤壳出现了变形的状况,同样也是会造成泄漏现象发生的,在此建议,在开展测试之前,先用干燥的气体进行保压操作,以此来检查设备的气密性。要是扩散流的数值持续呈现出偏高的态势,那么很有可能是膜孔出现了局部破损的问题,这种时候,就需要结合批次记录来评估一下是不是要更换滤芯了。每一次测试失败的时候,都应当十分详细地记录下操作所涉及的参数,从而为后续的偏差调查提供相应的依据。
各国药典以及GMP指南都清楚明确地要求,要针对呼吸器滤芯,在使用之前、使用之后开展完整性测试。美国FDA的cGMP以及欧盟EMA的附录1均着重强调,测试报告一定要涵盖测试方法、合格标准、仪器编号、操作人员以及原始数据打印条。在实际进行审核时,常常会发觉企业仅仅保存了“合格”结论,然而却缺失原始曲线图,这在合规性方面属于重大缺陷,建议采用带有审计追踪功能的自动化测试设备,以此来确保数据完整性以及可追溯性。
在平常的操作期间,你有没有碰到过测试的结果呈现出反复无常的状况,又或者是和滤芯材质特性存在关联的疑难情形呢?欢迎于评论区之中分享你开展排查的经验,一块儿去探讨更为实用的解决办法。
联系电话
微信扫一扫
